G2329S Index: Food Science & Technology


José Rodrigo Mendoza, Post-Doctoral Research Associate
Andréia Bianchini, Associate Professor
El maíz (Zea mays) es un alimento básico en México y en Centro y Suramérica, con un rápido aumento en su consumo en Europa y Estados Unidos (2, 10). Este producto agrícola es propenso a sufrir daños por mohos debido a prácticas de manejo pre- y post- cosecha inadecuadas, lo que puede conducir a una reducción del rendimiento y calidad. Además, la presencia de ciertos mohos suele ir acompañada de contaminación por micotoxinas, lo cual puede comprometer la inocuidad del maíz. Las micotoxinas se definen como metabolitos secundarios de hongos filamentosos (mohos), predominantemente pertenecientes a los géneros Alternaria, Aspergillus, Claviceps, Fusarium, y Penicillium (9).
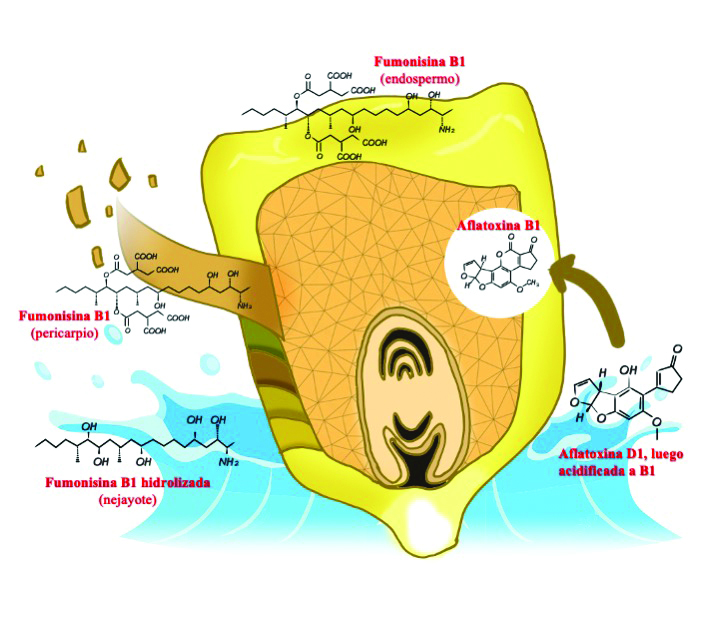
Fig. 1. Ejemplificación del destino hipotético de algunas micotoxinas durante la nixtamalización del maíz. Algunas micotoxinas pueden solubilizarse parcialmente, mientras que en otros casos pueden estar enmascaradas y seguir presentes en los alimentos.
La exposición de micotoxinas en humanos y animales se lleva a cabo principalmente a través de los alimentos y puede provocar intoxicaciones agudas o crónicas, conocidas como micotoxicosis, con síntomas que varían según la dosis, la duración de la exposición, el tipo de toxina, así como la salud del individuo (31).
El control de las micotoxinas representa un desafío en todo el mundo, siendo más problemático en regiones tropicales y subtropicales. Los dos principales grupos de toxinas fúngicas que afectan al maíz son las aflatoxinas y la fumonisinas (3, 25). Sin embargo, también se han reportado otras toxinas en maíz como zearalenona, deoxinivalenol, citrinina y ocratoxina (9, 20, 24). Más información sobre micotoxicosis en NebGuide Comprendiendo las toxinas (micotoxinas) fúngicas (mohos)—disponible en inglés, G1513.
La nixtamalización es un método originario de Mesoamérica que consiste en una cocción alcalina (cal, Ca(OH)2) de maíz. La solución alcalina degrada y elimina el pericarpio, suaviza la estructura del endospermo y permite la difusión de agua e iones de calcio en la porción interna de almidón del grano, lo cual puede a su vez influir en la contaminación de micotoxinas (Figura 1). En el proceso tradicional de nixtamalización (Figura 2), después de la cocción alcalina, los granos de maíz se dejan en reposo durante aproximadamente 24 h, y luego se lavan para eliminar los restos del pericarpio y el exceso de calcio (8, 10, 19).
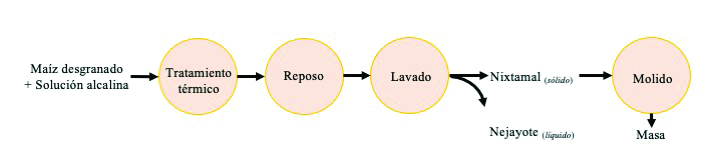
Fig. 2. Proceso tradicional de nixtamalización y elaboración de masa
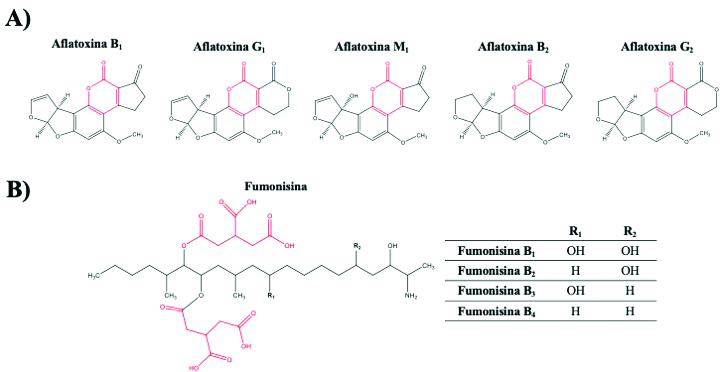
Fig. 3. Ejemplos de estructuras químicas de aflatoxinas y fumonisinas. El anillo de lactona en la aflatoxina y las fracciones de ácido tricarbalílico de la fumonisina están marcados en rojo.
El producto resultante, llamado nixtamal, se muele para producir la masa, la cual es la base de varios platillos como tortillas, tamales, masa rellena (e.g. pupusas, arepas), bebidas (e.g. atol, pozol) y alimentos tipo snack. Además de los cambios sensoriales, la nixtamalización mejora el valor nutricional del maíz ya que aumenta el contenido de calcio, aumenta la biodisponibilidad de la niacina, y reduce los niveles de ácido fítico (2, 27). Además, la nixtamalización puede afectar los niveles de micotoxinas en el producto alimenticio resultante. Los efectos sobre las aflatoxinas y fumonisinas presentes en el maíz contaminado sometido a este tratamiento térmico alcalino se discuten en esta publicación.
Las fumonisinas (Figura 3B) son micotoxinas producidas principalmente por Fusarium verticillioides y F. proliferatum. Las formas generalmente presentes en alimentos contaminados forman parte de la serie B, específicamente fumonisina B1 (FB1), B2 (FB2), B3 (FB3) y B4 (FB4) (16). De estas, la Agencia Internacional para la Investigación del Cáncer (IARC) ha clasificado a la FB1 como un “carcinógeno del Grupo 2B”, lo que indica que esta toxina es posiblemente carcinógena en seres humanos (4). Las fumonisinas son termoestables (100–120°C), especialmente a pH neutro, siendo capaces de tolerar diversos tratamientos térmicos comúnmente usados en el procesamiento y preparación de alimentos (12, 13). La Tabla 1 incluye algunos hallazgos de los efectos que tiene la nixtamalización sobre las fumonisinas.
Tabla 1. Ejemplos sobre efectos de diferentes condiciones de nixtamalización en la reducción de fumonisinas. Partes por millón (ppm) = miligramos de fumonisina por kilogramo (mg/kg) de masa de maíz.
|
Tipo de fumonisina (FB) |
Parámetros de proceso |
Método de cuantificación |
Incremento o reducción de fumonisina en masa |
Observaciones |
Ref. |
|---|---|---|---|---|---|
|
FB2, 5 ppm |
pH 10, 175–200°C, Calentamiento por 60 min |
HPLC |
Hasta 90% de reducción de FB2 |
Reducción independientemente del pH 4–10. Procesamiento mínimo recomendado: 150°C, 60 min. |
(12) |
|
FB1, 8.8 ppm |
pH 10, 100–125°C, 5 min de vapor |
HPLC |
Reducción de 89.5% FB1 |
Base seca. Las fumonisinas hidrolizadas (HFB) fueron los principales compuestos de descomposición detectados. |
(6) |
|
LDD: 0.01 ppm |
Incremento de 8.4% HFB1 |
||||
|
FB1, 34.6 ppm |
pH alcalino. Patentado, propietario. |
HPLC, LC-MS |
Reducción 86.4% FB1 |
FB1 parcialmente hidrolizada (PHFB1) encontrada principalmente en desechos líquidos y sólidos. |
(29) |
|
PHFB1, 1.34 ppm |
Reducción 32.8% PHFB1 |
||||
|
HFB1, 0.95 ppm |
Reducción 5.5% HFB1 |
||||
|
FB1, 0.7–1.65 ppm |
pH 10.6–11.1 15–60 min hervido |
HPLC |
Reducción 80–100% FB1 |
La FB1 disminuyó a medida que incrementó la cal. El tiempo de ebullición no tuvo ningún efecto aparente. |
(5) |
|
LDD: 0.025 ppm |
|||||
|
FB1, 38.1 ppm |
105 min hervido |
HPLC, LC-MS |
Reducción de fumonisinas totales del 50% |
Las FB1/HFB1 totales en el agua de cal residual y los lavados con agua representaron el 50% del total de FB1 en el maíz crudo. |
(21) |
|
LDD: 0.025 ppm |
Tabla 2. Ejemplos sobre efectos de diferentes condiciones de nixtamalización en la reducción de aflatoxinas. Partes por billón (ppb) = microgramos de aflatoxina por kilogramo (mg/kg) de masa de maíz.
|
Tipo de aflatoxina (AF) |
Parámetros de proceso |
Método de cuantificación |
Incremento o reducción de aflatoxina en masa |
Observaciones |
Ref. |
|---|---|---|---|---|---|
|
Aflatoxina total |
~pH 10 (nejayote) |
Fluorometría |
Tradicional: 52–85% red. aflatoxina total |
La mayor parte de la modificación y desintoxicación de aflatoxinas se produjo en el licor de cocción debido al pH elevado. |
(26) |
|
98°C |
|||||
|
Tradicional: 40 min hervido |
|||||
|
Comercial: Reposo directo |
Comercial: 30–71% red. aflatoxina total |
||||
|
Aflatoxina total, 678.3 ppb |
pH 8.24 35 min a 85°C |
HPLC |
93.2% reducción |
La acidificación provocó la reformación de la aflatoxina original en la masa de maíz. |
(18) |
|
LDD: 0.5 ppb |
57.2% incremento |
||||
|
Aflatoxina total, Nivel 1: 29 ppb, Nivel 2: 93 ppb |
Tradicional: 0.99% cal (w/v) 70 min a 85°C |
HPLC |
Tradicional: Nivel 1: 89% red. Nivel 2: 87% red. |
La nixtamalización ecológica utiliza menos agua y utiliza el grano integral. |
(17) |
|
Ecológica: 0.37% cal (w/v). 10 min a 92°C |
LDD: 0.5 ppb |
Ecológica: Nivel 1: 25% red. Nivel 2: 13% red. |
|||
|
AFB1, 495 ppb AFM1, 402 ppb AFB1 dihidro-diol, 30.4 ppb |
0.3% cal (w/w) 30 min a 90–96°C |
HPLC |
94.2% red. AFB1 |
La adición de 3% de H2O2 resultó en una mayor reducción de AFB1 |
(7) |
|
94.5% red. AFM1 |
|||||
|
LDD: 5 ppb AFB1, 15 ppb AF total |
92.8% red. AFB1 di-hidrodiol |
El pH elevado (alcalino) del proceso de nixtamalización promueve la ionización de los grupos hidroxilo del almidón, así como la hidrólisis de la molécula de fumonisina original (6) al eliminar los grupos de ácido carboxílico. Algunos bioensayos de alimentación en ratas han tenido como objetivo evaluar la eficacia desintoxicante de la nixtamalización. A diferencia de FB1, la FB1 hidrolizada (HFB1) no causó defectos del tubo neural (30). Durante el procesamiento de alimentos, las fumonisinas pueden crear enlaces con varios componentes dentro de la matriz alimentaria (por ejemplo, el nixtamal) o reaccionar con otros ingredientes, como azúcares reductores. Las micotoxinas enlazadas pueden ser un problema ya que pueden enmascararse y permanecer indetectables por métodos convencionales, lo que da como resultado una subestimación de la toxicidad (total) potencial de los productos contaminados. Hallazgos recientes (4) indican que las fumonisinas cuantificadas en el agua de remojo (nejayote) y masa, durante la nixtamalización, representaron más de lo que se cuantificó inicialmente en los granos de maíz, evidenciando formas de fumonisinas asociadas a la matriz que fueron liberadas durante el procesamiento.
Las fumonisinas son solubles en agua y, en consecuencia, la nixtamalización puede reducir el contenido de fumonisinas de los productos alimenticios si se desecha el nejayote (23), reduciendo así el potencial hepatotóxico y nefrotóxico de la masa contaminada y los productos derivados hechos de maíz contaminado (28). Además, la FB1 parcialmente hidrolizada (PHFB1) y HFB1 formadas durante la nixtamalización tienden a encontrarse principalmente en el líquido de cocción/remojo y en los desechos sólidos. Asimismo, la cantidad de FB1 en la masa y las tortillas tiende a disminuir con los aumentos relativos de cal, en donde el tiempo de ebullición no tiene ningún efecto aparente (29). A concentraciones más elevadas de cal, más pericarpio tiende a ser removido, lo que resulta en niveles reducidos de fumonisinas. La nixtamalización, junto con el lavado, son cruciales para reducir la presencia de fumonisinas en el producto final, mientras que el molido, formado, horneado de la masa tienen poco o menor impacto. La reducción de fumonisinas durante el procesamiento puede indicar que estas son extraídas o removidas de los productos, destruidas, o modificadas químicamente ligándose a componentes de la matriz, o en fracciones inextraíbles (11).
Las aflatoxinas (Figura 3A) son compuestos tóxicos y hepatocarcinogénicos producidos por la mayoría de las cepas de Aspergillus parasiticus y algunos de los mohos A. flavus. Las aflatoxinas (AF) que se encuentran en los granos incluyen B1, B2, G1, and G2 (16), de las cuales la AFB1 es el carcinógeno hepático natural más potente conocido (15). Las aflatoxinas son resistentes a la inactivación térmica, con una temperatura de descomposición que oscila entre 237–306°C, aunque esto puede variar según la disponibilidad de agua y el pH (16, 26). Se ha sugerido que la presencia de humedad en las matrices alimentarias facilita la apertura del anillo de lactona en AFB1, permitiendo la formación de un ácido carboxílico terminal que a su vez permite una degradación mediante descarboxilación inducida por calor (13). Las condiciones alcalinas promueven la degradación térmica a través del aumento de la solubilidad de las aflatoxinas (Tabla 2). Sin embargo, el pH dentro de los granos no aumenta significativamente en comparación con la solución de cal circundante. Por lo tanto, es probable que sólo la toxina ubicada en las capas externas de los granos pueda solubilizarse en la fracción de nejayote, potencialmente mejorando la inocuidad de la masa. Sin embargo, la apertura del anillo de lactona puede ser un fenómeno reversible. Las aflatoxinas modificadas en los productos derivados de la masa se pueden revertir a su forma original mediante la acidificación en el tracto digestivo durante la digestión (23, 26). Elias-Orozco et al (7) demostraron que la adición de peróxido de hidrógeno al 3% (H2O2) a la mezcla de maíz y agua resultó en una mayor reducción de AFB1 que cuando cada tratamiento, cal o H2O2, se aplicó de forma independiente. Este fenómeno posiblemente se deba a la reacción de la cal con el anillo de lactona y a la interacción entre el H2O2 y el doble enlace en el anillo de furano de la molécula de aflatoxina. A pesar del potencial de este tratamiento, esta adición compromete la palatabilidad de la masa y los productos derivados.
Aparte de las fumonisinas y aflatoxinas, existen otras micotoxinas que se pueden encontrar en el maíz. El deoxinivalenol (vomitoxina, DON) y sus derivados son micotoxinas producidas por ciertas especies del moho Fusarium que infectan frecuentemente al maíz, trigo y otros granos. Se ha reportado que el DON se reduce significativamente después de la nixtamalización debido a su inestabilidad en condiciones alcalinas. De manera similar a lo que se observa con las fumonisinas, la capa externa de los granos de maíz contaminados contiene una alta cantidad de DON, por lo que la remoción del pericarpio durante el proceso de nixtamalización ayuda a la reducción de este contaminante (14). Abbas et al (1) reportaron que la zearalenona, una micotoxina estrogénica producida por algunas especies de Fusarium, puede sufrir una reducción del 59–100% en maíz contaminado después de la nixtamalización. El mismo grupo también informó una pérdida de 72–82% de DON, así como una reducción total (100%) de 15-acetil-DON en muestras de maíz después de la cocción alcalina. También se ha evaluado la reducción de moniliformina a través de la cocción alcalina del maíz (22) y se observó una reducción del 71% de la toxina durante el proceso de nixtamalización.
La reducción de micotoxinas en procesos como la nixtamalización es variable, ya que depende de varios parámetros que no se limitan al tiempo de cocción, temperatura, pH, e ingredientes alimentarios. Durante la nixtamalización, tanto la eliminación del pericarpio como la solubilidad de las micotoxinas durante el reposo parecen estar directamente relacionadas con los niveles de contaminación encontrados en el producto final.
Si bien las micotoxinas pueden potencialmente controlarse hasta cierto punto mediante la nixtamalización por remoción, modificación química a compuestos menos tóxicos o degradación, se recomienda a los procesadores de alimentos que siempre utilicen materia prima de la mejor calidad posible, acorde a regulaciones regionales vigentes sobre micotoxinas. Aunque los métodos de procesamiento pueden ayudar a reducir la contaminación, garantizar la inocuidad de los productos a base de maíz debe depender principalmente del uso de granos, en la medida de lo posible, libres de micotoxinas.
1. Abbas, H. K., C. J. Mirocha, R. Rosiles, and M. Carvajal. 1988. Decomposition of zearalenone and deoxynivalenol in the process of making tortillas from corn. Cereal Chem.
2. Caballero-Briones, F., A. Iribarren, and J. Peña. 2000. Recent advances on the understanding of the nixtamalization process. Superf. y vacío 10:20–24.
3. Chulze, S. N. 2010. Strategies to reduce mycotoxin levels in maize during storage: a review. Food Addit. Contam. Part A. Chem. Anal. Control. Expo. Risk Assess. 27:651–7.
4. De Girolamo, A., V. M. T. Lattanzio, R. Schena, A. Visconti, and M. Pascale. 2016. Effect of alkaline cooking of maize on the content of fumonisins B1 and B2 and their hydrolysed forms. Food Chem. Elsevier Ltd 192:1083–1089.
5. De La Campa, R., J. D. Miller, and K. Hendricks. 2004. Fumonisin in tortillas produced in small-scale facilities and effect of traditional masa production methods on this mycotoxin. J. Agric. Food Chem. 52:4432–4437.
6. Dombrink-Kurtzman, M. A., T. J. Dvorak, M. E. Barron, and L. W. Rooney. 2000. Effect of nixtamalization (alkaline cooking) on fumonisin-contaminated corn for production of masa and tortillas. J. Agric. Food Chem. 48:5781–5787.
7. Elias-Orozco, R., A. Castellanos-Nava, M. Gaytán-Martínez, J. D. Figueroa-Cárdenas, and G. Loarca-Piña. 2002. Comparison of nixtamalization and extrusion processes for a reduction in aflatoxin content. Food Addit. Contam. 19:878–885.
8. Fernández-Muñoz, J. L., M. E. Rodríguez, R. C. Pless, H. E. Martínez-Flores, M. Leal, J. L. Martinez, and L. Baños. 2002. Changes in nixtamalized corn flour dependent on postcooking steeping time. Cereal Chem. 79:162–166.
9. Gullino, M. L., J. P. Stack, J. Fletcher, and J. D. Mumford. 2017. Practical Tools for Plant and Food Biosecurity, 8th ed. Springer, Cham, Switzerland.
10. Gutiérrez-Cortez, E., J. I. Rojas-Molina, M. L. Zambrano-Zaragoza, D. Quintanar-Guerrero, R. M. González-Reza, A. Rojas-Molina, and D. G. Espinosa-Arbeláez. 2013. Effect of processing conditions on the production of nixtamalized corn flours by the traditional method. CYTA—J. Food 11:46–53.
11. Humpf, H. U., and K. A. Voss. 2004. Effects of thermal food processing on the chemical structure and toxicity of fumonisin mycotoxins. Mol. Nutr. Food Res. 48:255–269.
12. Jackson, L. S., J. J. Hlywka, K. R. Senthil, and L. B. Bullerman. 1996. Effects of Thermal Processing on the Stability of Fumonisin B2 in an Aqueous System. J Agric Food Chem 44:1984–1987.
13. Kabak, B. 2009. The fate of mycotoxins during thermal food processing. J. Sci. Food Agric. 89:549–554.
14. Kaushik, G. 2015. Effect of Processing on Mycotoxin Content in Grains. Crit. Rev. Food Sci. Nutr. 55:1672–1683.
15. Lee, H. J., and D. Ryu. 2015. Advances in Mycotoxin Research: Public Health Perspectives. J. Food Sci. 80:T2970–T2983.
16. Magan, N., and M. Olsen. 2004. Mycotoxins in food: detection and control, 1st ed. CRC Press.
17. Méndez-Albores, J. A., G. Arámbula-Villa, M. G. Loarca-Piña, J. González-Hernández, E. Castaño-Tostado, and E. Moreno-Martínez. 2004. Aflatoxins’ fate during the nixtamalization of contaminated maize by two tortilla-making processes. J. Stored Prod. Res. 40:87–94.
18. Méndez-Albores, J. A., G. A. Villa, J. C. Del Rio-García, and E. M. Martínez. 2004. Aflatoxin-detoxification achieved with Mexican traditional nixtamalization process (MTNP) is reversible. J. Sci. Food Agric. 84:1611–1614.
19. Méndez-Montealvo, G., F. J. García-Suárez, O. Paredes-López, and L. A. Bello-Pérez. 2008. Effect of nixtamalization on morphological and rheological characteristics of maize starch. J. Cereal Sci. 48:420–425.
20. National Corn Growers Association. 2018. Mycotoxins: What is a Mycotoxin, Aflatoxin, Fumonisin. Mycotoxin Inf.
21. Palencia, E., O. Torres, W. Hagler, F. I. Meredith, L. D. Williams, and R. T. Riley. 2003. Total fumonisins are reduced in tortillas using the traditional nixtamalization method of mayan communities. J. Nutr. 133:3200–3203.
22. Pineda-Valdes, G., D. Ryu, D. S. Jackson, and L. B. Bullerman. 2002. Reduction of moniliformin during alkaline cooking of corn. Cereal Chem. 79:779–782.
23. Ryu, D., A. Bianchini, and L. B. Bullerman. 2008. Effects of processing on mycotoxins. Stewart Postharvest Rev. 4.
24. Shotwell, O. L. 1991. Natural Ocurrence of Mycotoxins in Corn, p. 325. In Mycotoxins and Animal Foods. CRC Press, Boca Raton, Florida.
25. Torres, O., J. Matute, J. Gelineau-van Waes, J. R. Maddox, S. G. Gregory, A. E. Ashley-Koch, J. L. Showker, K. A. Voss, and R. T. Riley. 2015. Human health implications from co-exposure to aflatoxins and fumonisins in maize-based foods in Latin America: Guatemala as a case study. World Mycotoxin J. 8:143–159.
26. Torres, P., M. Guzmán-Ortiz, and B. Ramírez-Wong. 2001. Revising the role of pH and thermal treatments in aflatoxin content reduction during the tortilla and deep frying processes. J. Agric. Food Chem. 49:2825–2829.
27. Valderrama-Bravo, C., A. Rojas-Molina, E. Gutiérrez-Cortez, I. Rojas-Molina, A. Oaxaca-Luna, E. De la Rosa-Rincón, and M. E. Rodríguez-García. 2010. Mechanism of calcium uptake in corn kernels during the traditional nixtamalization process: Diffusion, accumulation and percolation. J. Food Eng. Elsevier Ltd 98:126–132.
28. Voss, K. A., C. W. Bacon, F. I. Meredith, and W. P. Norred. 1996. Comparative Subchronic Toxicity Studies of Nixtamalized and Water-extracted Fusarium moniliforme Culture Material. Food Chem. Toxicol. 34:623–632.
29. Voss, K. A., S. M. Poling, F. I. Meredith, C. W. Bacon, and D. S. Saunders. 2001. Fate of fumonisins during the production of fried tortilla chips. J. Agric. Food Chem. 49:3120–3126.
30. Voss, K., D. Ryu, L. Jackson, R. Riley, and J. Gelineau-Van Waes. 2017. Reduction of Fumonisin Toxicity by Extrusion and Nixtamalization (Alkaline Cooking). J. Agric. Food Chem. 65:7088–7096.
31. Wild, C. P., and Y. Y. Gong. 2009. Mycotoxins and human disease: A largely ignored global health issue. Carcinogenesis 31:71–82.
This publication has been peer reviewed.
Nebraska Extension publications are available online at http://extensionpubs.unl.edu/.
Extension is a Division of the Institute of Agriculture and Natural Resources at the University of Nebraska–Lincoln cooperating with the Counties and the United States Department of Agriculture.
Nebraska Extension educational programs abide with the nondiscrimination policies of the University of Nebraska–Lincoln and the United States Department of Agriculture.
© 2021, The Board of Regents of the University of Nebraska on behalf of the Nebraska Extension. All rights reserved.